Brasil
Ministério envia à Anvisa informações sobre autotestes de covid-19
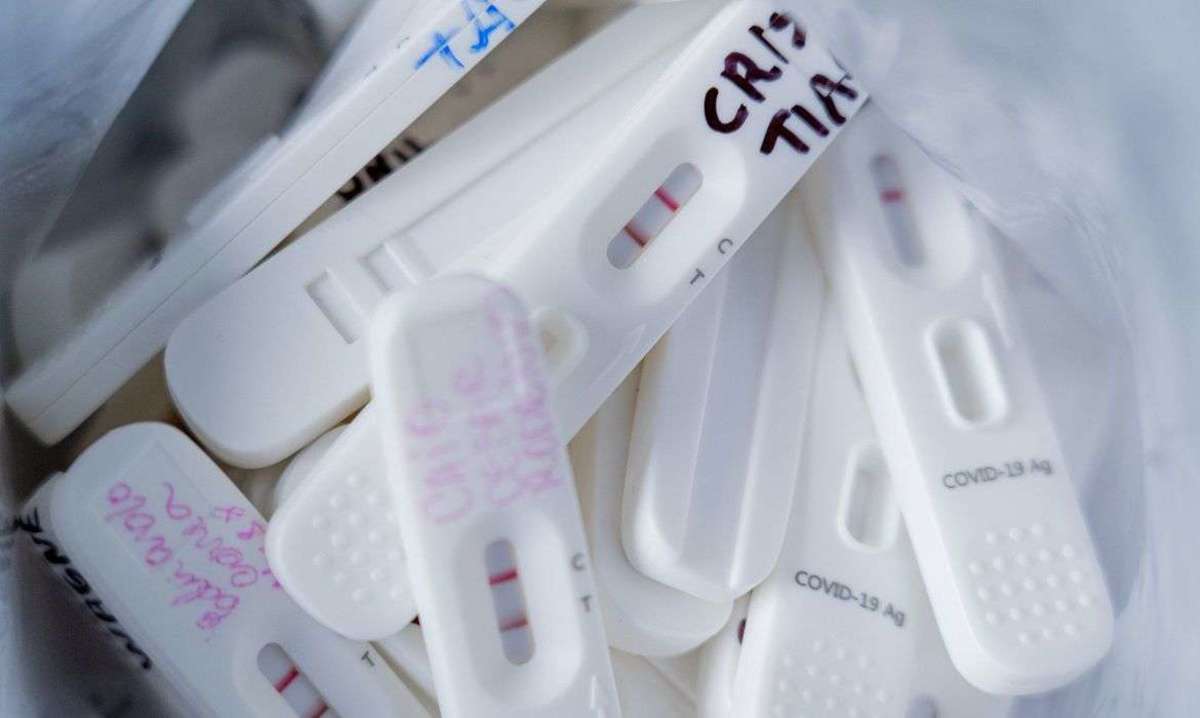
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu do Ministério da Saúde (MS) informações sobre política pública para implementação dos autotestes de diagnóstico de covid-19. As informações, de acordo com o ministério, foram encaminhadas à agência reguladora ontem (25) à noite.
A agência confirmou o recebimento e disse que vai analisar as informações, mas não há prazo para resposta. Acrescentou, no entanto, que a deliberação sobre venda de autotestes deve sair no menor tempo possível.
A liberação de autotestes foi solicitada à Anvisa no dia 13 de janeiro. Na semana passada, a agência adiou a decisão e solicitou informações sobre como os testes seriam usados por pacientes leigos e como será feita a notificação dos resultados à Rede Nacional de Dados em Saúde do governo federal. Portaria do ministério determina que notificações de casos de covid-19 são compulsórias.
O ministério argumenta que a liberação dos testes vai ajudar no diagnóstico e tratamento da doença e que, se liberados, os autotestes devem integrar o Plano Nacional de Expansão da Testagem (PNE-Teste) para Covid-19.
“Se aprovada, medida será mais um eixo de apoio ao diagnóstico e monitoramento da situação epidemiológica do país. A orientação ao público sobre manuseio dos testes, conduta do usuário após o resultado e notificação do diagnóstico serão incluídos na nova edição do PNE-Teste”, informou o MS.
Nesta quarta-feira (26), a Anvisa determinou o recolhimento de mais um autoteste de covid-19 – o meuDNA PCR-LAMP Autocoleta de Saliva, da empresa Empreendimentos Pague Menos S/A. Ontem (25), a agência suspendeu a comercialização distribuição, fabricação, importação, propaganda e uso do Autoteste Covid-19 Isa Lab.
Em nota, a Anvisa informou que, “até o momento, não existe nenhum produto aprovado como autoteste, ou seja, para uso por usuários leigos”.
Posicionamentos
Em nota enviada à Agência Brasil, a Isa Lab informou que o kit citado na matéria é um teste de detecção de covid-19 que utiliza como base do diagnóstico a técnica PCR-LAMP (Amplificação Isotérmica Mediada por Loop) a partir de uma amostra de saliva, que é coletada pelo próprio paciente.
“Portanto, trata-se de um teste de autocoleta e não um autoteste. Essa é uma maneira de testagem da infecção ativa, apontada pela Organização Mundial da Saúde (OMS) como a melhor ferramenta para rastrear o vírus e impedir a transmissão. Da mesma forma como acontece com o RT-PCR, o teste considerado “padrão ouro”, a técnica PCR-LAMP identifica o RNA do vírus nas células da pessoa infectada desde a fase inicial. E, apesar da amostra de saliva ser coletada pelo paciente, ela é encaminhada para a Mendelics, um laboratório de análises clínicas, líder em genômica no Brasil, devidamente registrado (CRM-SP 955.471) e acreditado (PALC 32290508, CGCRE Inmetro – Norma 15189:2015 – CLC 0007). É no laboratório que é realizada a análise e liberação de resultado”, traz a nota.
Segundo a empresa, o kit está registrado na Anvisa e está de acordo com a legislação e regulamentação vigentes. “A embalagem do produto foi desenvolvida quando a categoria de autotestes ainda não se fazia uma realidade no mundo. Por fim, até que haja uma reavaliação do entendimento da Anvisa quanto à suspensão presente, a Isa Lab retirou o produto de comercialização e reforça seu compromisso com a segurança e bem-estar dos clientes, que contam com um atendimento atestado pelo certificado ONA – uma metodologia de acreditação desenvolvida em 1999, a partir de métodos de certificação regionais da América Latina e de outros países, como Estados Unidos, Canadá, Espanha e Inglaterra, que tem por objetivo geral estimular o desenvolvimento de um processo permanente de avaliação e certificação da qualidade dos serviços de saúde”, completa a nota.
A empresa meuDNA também enviou nota à Agência Brasil em que afirma que o kit de coleta de saliva vendido em farmácias é um produto registrado na Anvisa e está de acordo com a legislação e regulamentação vigentes. Segundo a empresa, o kit é utilizado para autocoleta domiciliares de amostras e subsequentemente são analisadas em laboratórios de análises clínicas.
“O teste meuDNA Covid não se trata de um autoteste ou de teste rápido. Não há testagem realizada pelo paciente ou pelo farmacêutico. O teste meuDNA Covid é um teste laboratorial com fim diagnóstico, realizado no laboratório Mendelics. A Mendelics é um laboratório de análises clínicas, líder em genômica no Brasil, devidamente registrado (CRM-SP 955.471) e acreditado (PALC 32290508, CGCRE Inmetro – Norma 15189:2015 – CLC 0007). Os testes realizados pela Mendelics são regidos pela RDC 302/2005 da Anvisa. O teste meuDNA disponível em farmácias e no site meudna.com utiliza como base do diagnóstico a técnica PCR-LAMP (Amplificação Isotérmica Mediada por Loop). Assim como o RT-PCR, o teste considerado “padrão ouro”, ela identifica o RNA do vírus nas células da pessoa infectada desde a fase inicial. Ou seja, trata-se de uma maneira de testagem da infecção ativa, apontada pela Organização Mundial da Saúde (OMS) como a melhor ferramenta para rastrear o vírus e impedir a transmissão”, diz a nota.
A empresa disse ainda que espera que a Anvisa reavalie a “interpretação errônea e libere novamente os kits de autocoleta” o mais rápido possível.
Matéria atualizada às 17h44 para acréscimo de posicionamento das empresas meuDNA e Isa Lab.